·
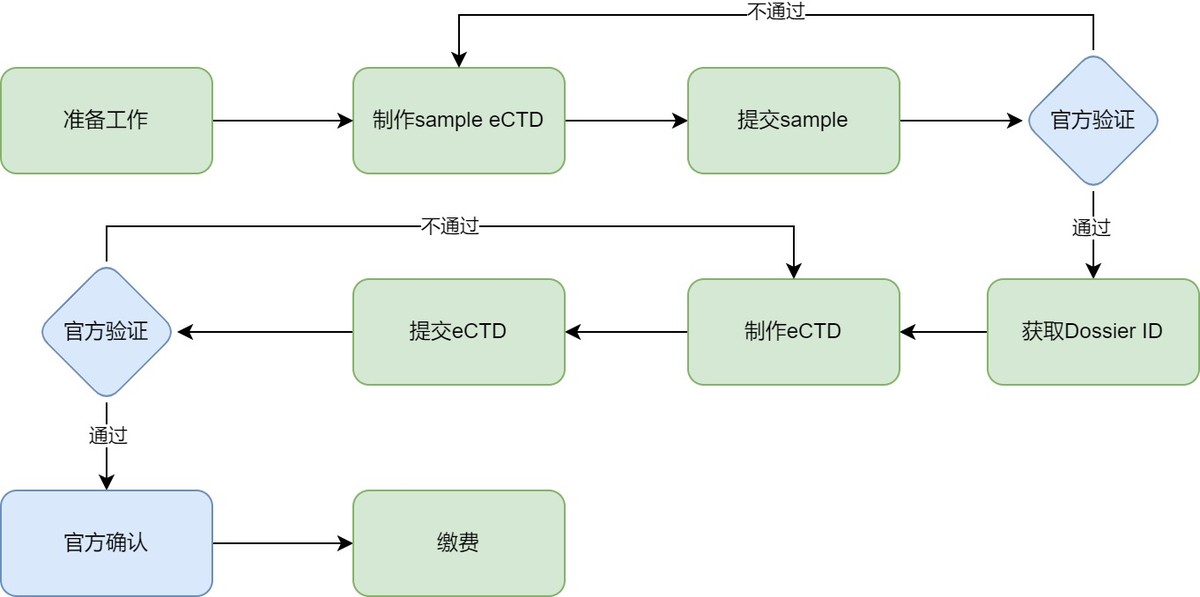
1. 准备工作
准备sample eCTD的相关文件,如cover letter,申请表,授权信等;
2. 制作sample eCTD
根据官方指南(Preparation of Regulatory Activities in the Electronic Common Technical Document (eCTD) Format)制作DMF的sample eCTD文件;
3. 提交sample
通过CESG(Common Electronic Submissions Gateway)提交sample eCTD;
4. 官方验证
提交后,向官方发送邮件确认提交,验证不通过时,按照官方的回复邮件修改sample eCTD并重新提交;
5. 获取Dossier ID
sample eCTD验证通过后,可在Health Canada官网在线申请Dossier ID;
6. 制作eCTD
获取Dossier ID后,按照sample eCTD制作正式提交版的DMF eCTD文件;
7. 提交eCTD
通过CESG(Common Electronic Submissions Gateway)提交eCTD;
8. 官方验证
提交后,等待官方确认,验证不通过时,按照官方的回复邮件修改 eCTD并重新提交;
9. 官方确认
eCTD验证通过后会收到两个文件:
1)ACKNOWLEDGMENT OF INFORMATION RECEIVED - MASTER FILE (MF)
2)INVOICE
10. 缴费
根据官方邮件中的发票和缴费方式,缴纳DMF相关费用。
